
콘텐츠
카탈라아제는 동물, 식물 및 호기성 박테리아의 세포에서 발견되는 효소입니다. 효소는 세포에서 합성되어 반응에서 촉매 역할을하는 큰 분자입니다. 효소의 각 유형은 특정 기능을 수행하며, 카탈라아제의 기능은 잠재적으로 유해한 부산물을 세포에 유용한 요소로 변환하는 것입니다.

기능
대부분의 효소와 마찬가지로 카탈라아제도 단백질입니다. 막 세포 소기관 인 페 록시 좀 (peroxisomes)에서 발견됩니다. 카탈라아제는 중요한 생물학적 기능을 가지고 있습니다. 그것은 유기체에 유해한 물질 인 과산화수소를 물과 분자 산소로 분해하는데 촉매 역할을합니다.이 물질은 무해하고 유용합니다.

구조
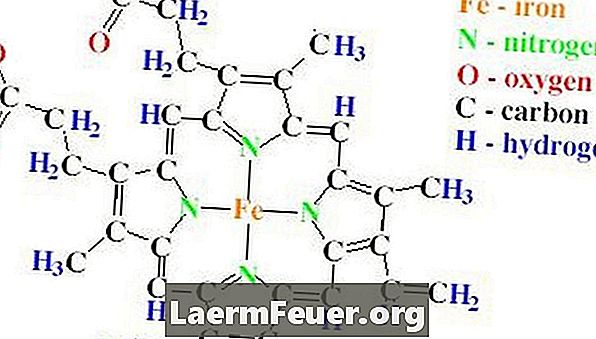
카탈라아제의 덤벨 구조는 각각 500 개 이상의 아미노산을 포함하는 4 개의 폴리 펩타이드 사슬을 포함합니다. 카탈라아제는 또한 protoporphyrin 고리로 만들어지며 하나의 철 원자를 포함하는 4 개의 heme 그룹을 가지고있다. 이 고리는 4 개의 사슬 안에 있습니다.
카탈라아제의 중요성
과산화수소는 유기체의 많은 생물학적 기능의 부산물입니다. 모든 호기성 유기체는 호흡에 산소를 사용합니다. 물의 산소 감소는 종종 불완전하고, 금속 이온으로부터의 여분의 전자가 전달되어 과산화물 형성을 일으킬 수 있습니다. 그러나, 대부분의 과산화수소는 미토콘드리아에서 ATP를 생산하는 과정에서 생성됩니다. 과산화수소가 살아있는 세포에 독성이 있지만, 물과 산소로 다시 분해하는 반응은 빠르고 효과적으로 일어납니다. 카탈라아제는 가장 효율적인 효소 중 하나로 알려져 있으며, 약 200,000 이벤트 / 초 / 하위 단위의 매출을 보입니다. 반응 속도를 증가시키는 카탈라아제가 없으면 과산화수소가 남아 세포를 손상시킵니다.
카탈라아제의 효과에 영향을 미치는 요인들
카탈라아제 및 이의 활성 비율은 온도, pH, 염 농도, 기질의 양 및 억제제 또는 활성제의 존재를 포함하는 여러 요인에 의해 변경된다. 고온은 효소의 변성을 일으킬 수 있기 때문에 온도는 모든 생화학 반응에서 중요한 요소입니다. 효소가 변성되면, 효소는 그 구조를 변화시켜 기질이 덜 효율적으로 결합하여 반응 속도를 감소시킨다. 한편, 최대 온도 (각 유형의 카탈라제마다 다르다)에 도달 할 때까지, 반응 속도는 온도와 함께 증가 할 것이다. pH, 산도 또는 용액에서 수소 이온의 농도는 0 ~ 14의 등급으로 측정됩니다. 용액이 더 산성이되면 (7 이하), 효소는 용액에서 수소 이온을 얻을 수 있습니다 용액이 더 염기성이되면 (7 이상) 수소 이온이 손실 될 수 있습니다. 카탈라제 화학 결합이 변하기 때문에 이들 극한값은 반응 속도를 감소시킬 수 있습니다. 저해제는 활성 사이트가 아닌 사이트에 결합하는 비경쟁 저해제와 카탈라아제의 활성 사이트에 결합하는 경쟁 저해제의 두 가지 유형이 있습니다. 구리 황산염은 카탈라아제의 비 경쟁적 저해제로 알려져 있으며 시안화물은 경쟁력있는 억제제로 알려져 있습니다. 일반적으로, 과산화수소의 양이 증가함에 따라, 반응 속도 또한 증가 할 것이다. 그러나 효소 반응은 모든 반응이 최대 반응 속도에서 더 많은 기질을 첨가하면 더 이상 영향을 미치지 않는다는 것을 의미하는 포화 점에 도달한다는 Michaelis-Menten 방정식을 따른다.
카탈라아제의 다른 용도
카탈라아제는 사실상 모든 살아있는 유기체에 존재하기 때문에, 가장 잘 연구 된 효소 중 하나입니다. 이로 인해 과학자들은이 효소에 대한 다른 기능을 발견하게되었습니다. 카탈라아제는 식품 포장을 위해 플라스틱 내부를 처리하는 데 사용됩니다. 그것은 산화를 방지하고 따라서 음식을 보존하는 데 도움이됩니다. 카탈라아제는 과산화수소로 처리하여 우유와 치즈를 보존하는 과정 인 감기 멸균 과정에서도 사용됩니다. 이 효소는 잔류하는 과산화수소를 제거하는데 사용됩니다.