![[지식in] 정수의 구성적 정의 (정수와 연산)](https://i.ytimg.com/vi/VXakafYENhU/hqdefault.jpg)
콘텐츠
소자에는 전하가 없지만 이온은 양전하 또는 음전하를 가질 수 있습니다. 이것은 전자와 양성자의 수가 동일하기 때문에 두 입자가 생성하는 전하를 보상하기 때문입니다. 그러나 원소가 이온화되면 전자를 얻거나 잃게됩니다. 주기율표는 이들 중 하나의 이온이 양전하 또는 음전하를 띠는지 여부를 확인하는 것이 매우 쉬운 방식으로 이들 원소를 조직했습니다.
지침
-
왜 일부 원소는 전자를 잃고 다른 원소는 이온화되었을 때 얻는지를 이해하십시오. 최 외층이 가능한 많은 전자를 저장할 때 이들은 더 안정하다. 원소가 완전한 외층을 얻기 위해 전자를 잃는 것이 더 쉽다면, 이온화 할 때 전자가 그렇게 할 것이다. 요소가 외부 층을 채우기 위해 전자를 얻는 것이 더 쉬운 경우 반대가 발생합니다.
-
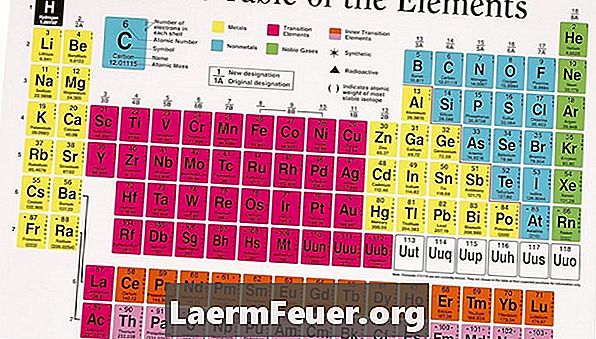
주기율표를보십시오. 그룹 (열) 1, 2, 3 및 14의 대부분의 원소는 이온화되면 양전하를.니다. 이는 전자가 원자 층 전체를 갖기 위해받는 것보다 전자를 덜 필요로하기 때문입니다. 따라서 음전하를 띤 전자를 잃는 것이 더 쉽습니다. 전자보다 양전하를 띄는 양성자가 더 많으므로 이들 이온은 양전하를.니다. 유타 주 딕시 스테이트 컬리지 (Dixie State College of Utah)에 따르면, 3 ~ 12 족 원소의 전이 금속은 항상 양전하를 띤다.
-
주기율표 15 족, 16 족 및 17 족을보고 음으로 하전 된 이온을 찾으십시오. 이들 원소의 대부분은 음전하를 띠면서 전리 수화물을 갖기 위해 잃어버린 전자보다 적은 전자를 얻을 필요가 있기 때문에 음전하를 띠게됩니다. 이 원소들은 전자를 얻으므로 이들의 이온은 양성자보다 더 많은 전자를 가지게되어 음전하를 띄게됩니다.
-
앞에서 언급 한 조언에 대한 예외 인 요소의 다양성에주의하십시오. 탄소와 같은 일부 원소는 절대로 이온을 형성하지 않습니다. 따라서, 이들 이온은 전하를 갖지 않는다. 포괄적 인 이온 차트에 대한 참조 소스 및 교과서를 참조하여 찾고있는 요소가 예외인지 확인하십시오.
필요한 것
- 주기율표